3月29日,諾華宣布美國 FDA 已為其 CAR- T 療法 CTL019(tisagenlecleucel-T)的生物制劑許可申請頒發了優先審評資格。這意味著諾華 CAR- T 生物制劑許可申請的審批流程有望得到進一步的縮減。
CTL019 zui初由賓夕法尼亞大學開發。2012 年,諾華與賓夕法尼亞大學達成合作協議,共同研究、開發與商業化包括 CTL019 在內的多項 CAR- T 療法,用以癌癥治療。目前,CTL019 申請上市的適應癥為兒童或年輕人中復發或難治性的急性 B 細胞型淋巴性白血病(B-cell acute lymphoblastic leukemia)

“在過去 5 年里,我們在癌癥的個體化治療上做出了大量努力,并在細胞工程的開發與應用上取得了巨大進展,” CAR- T 療法之一,賓夕法尼亞大學的 Carl June 教授說道:“現在我們知道,它能在范圍內的臨床試驗中治療患者,我們觀察到的試驗結果也表明對于那些常規療法不起作用的血液癌癥來說,它有望成為一種新的治療模式。”
在先前一項名為 ELIANA 的 2 期臨床試驗中,CTL019 取得了良好的療效。一共有 50 名患者參與了這項臨床試驗,而在接受 CTL019 治療的 3 個月后,高達 82% 的患者的癥狀出現了*緩解,或全血細胞計數不全的*緩解。治療后,沒有一名患者因“細胞因子風暴”(cytokine release syndrome)死亡。去年 12 月,這項研究也在美國血液學學會(American Society of Hematology)的大會上得到報道。
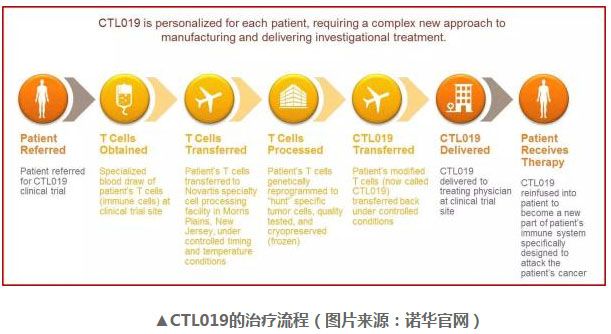
“CTL019 讓諾華站在了免疫細胞療法領域的科學與開發前沿,這是一種創新的療法,用以治療缺乏療法的特定癌癥,”諾華藥物開發負責人兼醫學官 Vas Narasimhan 博士說道:“CTL019 申請的接受與這項優先審評資格讓我們離為這些患者送上這一創新療法又更近了一步。”
請輸入賬號
請輸入密碼
請輸驗證碼
以上信息由企業自行提供,信息內容的真實性、準確性和合法性由相關企業負責,化工儀器網對此不承擔任何保證責任。
溫馨提示:為規避購買風險,建議您在購買產品前務必確認供應商資質及產品質量。